Che cos’è l’azoospermia?
L’azoospermia è una condizione clinica di infertilità maschile caratterizzata dall’assenza totale di spermatozoi nell’eiaculato. Si stima che tra il 10 % e il 15 % degli uomini con difficoltà a concepire presentino questa problematica.
In base all’origine del problema, l’azoospermia si suddivide principalmente in due categorie:
- Azoospermia ostruttiva (OA): circa il 30-40% dei casi. In questi pazienti la produzione degli spermatozoi nei testicoli è normale, ma vi è un’ostruzione lungo le vie seminali, che impedisce il loro passaggio.
- Azoospermia non ostruttiva (NOA) o secretoria: circa il 60-70%. Si tratta di un problema di produzione: i testicoli non riescono a produrre spermatozoi in modo efficace.
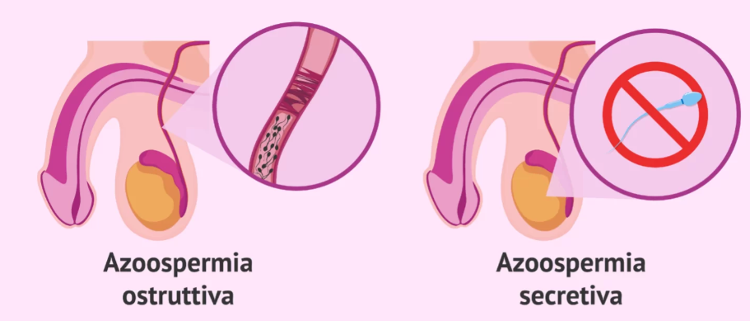 immagine:https://invitra.it/iniezione-intracitoplasmatica-degli-spermatozoi-icsi/
immagine:https://invitra.it/iniezione-intracitoplasmatica-degli-spermatozoi-icsi/
Quali sono le cause dell’azoospermia?
Le cause azoospermia sono molteplici e dipendono fortemente dal tipo (ostruttiva o non ostruttiva). Di seguito una panoramica più completa, con qualche approfondimento in più su fattori genetici, congeniti, infettivi, ormonali e ambientali.
-
Cause congenite o malformative
- Malformazioni congenite dei dotti seminali (per esempio assenza dei dotti deferenti), che possono causare ostruzione fin dalla nascita.
- Sindrome della “cellula di Sertoli” (Sertoli cell-only syndrome), in cui i tubuli seminiferi sono costituiti solo da cellule di Sertoli, senza cellule germinali: può portare a grave azoospermia secretoria.
- Anomalie cromosomiche: ad esempio microdelezioni del cromosoma Y o altre alterazioni che compromettono la spermatogenesi.
-
Danno testicolare / difetti di produzione
- Criptorchidismo: mancata discesa dei testicoli, che nel tempo può provocare atrofia testicolare.
- Orchiti, infiammazioni testicolari (anche per virus come le parotiti) che danneggiano la produzione spermatica.
- Varicocele: una dilatazione delle vene testicolari che può interferire con la spermatogenesi.
- Esposizione a tossine (veleni, sostanze chimiche, metalli pesanti) o a temperature elevate per lunghi periodi, che possono danneggiare le cellule produttrici di spermatozoi.
- Terapie farmacologiche: uso di farmaci citotossici (chemioterapia), steroidi anabolizzanti o altre terapie ormonali che interferiscono con la spermatogenesi.
-
Cause infettive o ostruttive
- Infezioni: processi infettivi come la tubercolosi genitale, la gonorrea o altre forme di epididimite / prostatite che possono causare cicatrici e ostruzioni.
- Interventi chirurgici pregressi: ad esempio la vasectomia, interventi per ernia inguinale o altre operazioni che possono danneggiare i dotti seminali e causare un blocco.
- Eiaculazione retrograda: lo sperma torna nella vescica invece di uscire, riducendo o annullando la quantità di spermatozoi misurabili nell’eiaculato.
-
Cause ormonali o genetiche legate alla spermatogenesi
- Ipogonadismo ipogonadotropo (disfunzione dell’asse ipotalamo-ipofisi), con ridotta stimolazione ormonale per la spermatogenesi.
- Sindrome di Klinefelter (caratterizzata da cromosoma X extra), che è una causa genetica nota di azoospermia non ostruttiva.
- Arresto maturativo: le cellule germinali nel testicolo non maturano fino a diventare spermatozoi, oppure si verifica una perdita delle cellule germinali.
- Cause idiopatiche: in molti casi non è identificabile una causa precisa, anche se possono esserci difetti genetici non ancora completamente compresi.
Sintomi
L’azoospermia non sempre dà sintomi evidenti: molti uomini risultano azoospermici solo dopo aver fatto accertamenti per infertilità.
Tuttavia, alcuni segni possono suggerire una forma ostruttiva o secretoria:
- Sintomi associabili all’azoospermia ostruttiva: spesso assenti squilibri ormonali; volume del testicolo normale, ma eiaculato ridotto.
- Sintomi generali: bruciore durante la minzione, pollachiuria (minzioni frequenti), presenza di sangue nello sperma, gonfiore (tumefazione) scrotale, infezioni ricorrenti o orchiti.
- Segmento secretorio / non ostruttivo: volume testicolare ridotto, alterazioni ormonali (es. FSH elevato), possono essere presenti anomalie del profilo ormonale.
Diagnosi
Per stabilire se sei affetto da azoospermia e per identificare le cause, il percorso diagnostico solitamente include:
- Esame del liquido seminale (spermiogramma) ripetuto almeno due volte a distanza di alcuni mesi.
- Analisi biochimica: ricerca di spermatozoi nelle urine dopo l’eiaculazione, per escludere un’eiaculazione retrograda.
- Anamnesi medica completa: indagare su eventuali interventi chirurgici (es. ernia), malattie genetiche, chemioterapia, traumi, infiammazioni genitali, fattori ambientali.
- Esame obiettivo: misurazione del volume testicolare (un testicolo piccolo può indicare una NOA, mentre un volume normale può suggerire un’ostruzione).
- Esami ormonali: dosaggio di FSH, testosterone, inibina-B, e, se necessario, analisi genetiche (cariotipo, microdelezioni del cromosoma Y).
- Ecografie:
- Ecografia transrettale della prostata per verificare ostruzioni dei dotti eiaculatori.
- Ecocolordoppler scrotale per escludere tumori testicolari.
- Biopsia testicolare: in casi selezionati, per valutare la presenza di spermatozoi nei tessuti e definire la presenza di spermatogenesi residua.
Cura e trattamento
Il trattamento dipende dal tipo di azoospermia (ostruttiva o non ostruttiva) e dalla causa sottostante:
- Azoospermia ostruttiva (OA):
- Tecniche microchirurgiche di ricanalizzazione (epididimo-vasostomia, vaso-vasostomia) per ripristinare la continuità delle vie seminali.
- Se la ricanalizzazione non è possibile o non funziona, è possibile recuperare spermatozoi da testicolo o epididimo tramite biopsia (TESE) per usarli nelle tecniche di fecondazione assistita (come ICSI).
- Azoospermia non ostruttiva (NOA):
- TESE (“Testicular Sperm Extraction”): prelievo chirurgico di una piccola porzione di tessuto testicolare da analizzare.
- Micro-TESE (biopsia testicolare microchirurgica): con microscopio, il chirurgo identifica le zone con potenziale residuo di spermatozoi, con percentuali di recupero più alte (intorno al 60-65%) e minor danno al tessuto.
- Tecniche alternative:
- PESA (Percutaneous Epididymal Sperm Aspiration) – aspirazione di spermatozoi dall’epididimo per via transcutanea.
- MESA (Microsurgical Epididymal Sperm Aspiration) – aspirazione microchirurgica.
- TESA (Testicular Sperm Aspiration) – aspirazione con ago dal testicolo.
- È importante tenere conto del profilo genetico: in alcune forme di NOA ci sono mutazioni o microdelezioni che possono essere trasmesse, perciò è consigliabile una consulenza genetica.