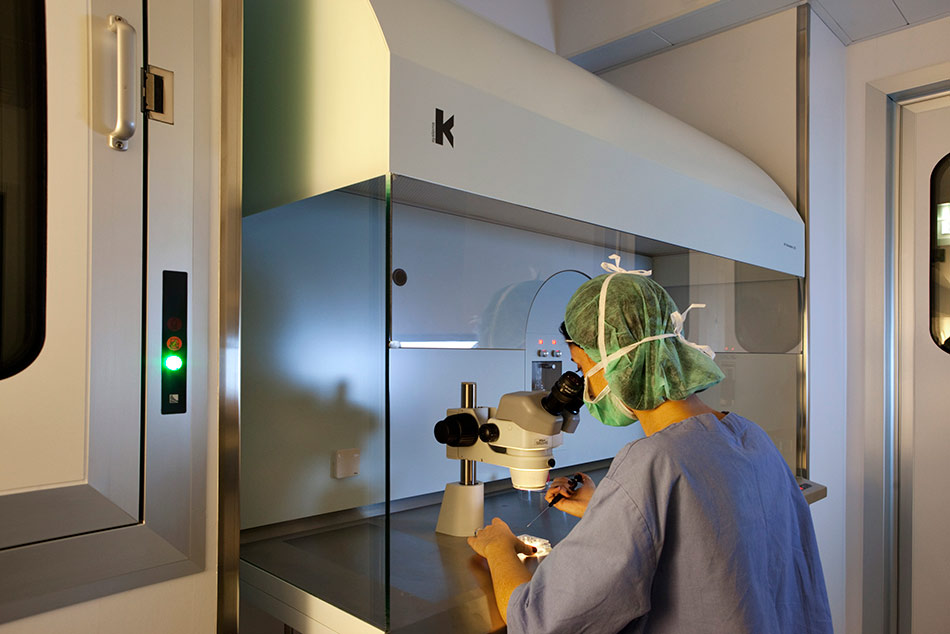
In cosa consiste l’hatching assistito
Ovociti ed embrioni nelle prime fasi di sviluppo sono circondati da un rivestimento acellulare, definito zona pellucida, costituito da glicoproteine, carboidrati e proteine zona pellucida–specifiche, la cui funzione si esplica sia durante i processi di fecondazione sia al termine degli stessi, quando impedisce la polispermia (penetrazione nell’ovocita da parte di altri spermatozoi), facilita il trasporto attraverso le tube degli ovociti fecondati e ne impedisce la dispersione dei blastomeri (cellule di divisione degli embrioni) così come il contatto con gli elementi cellulari che possono minarne l’integrità fino a quando non sia avvenuta la compattazione dei blastomeri.
Quando l’embrione raggiunge lo stato di blastocisti l’espansione della massa embrionale determina l’assottigliamento della zona pellucida, requisito fondamentale per l’interazione con l’endometrio e l’impianto dell’embrione.
Si osserva in vitro, tuttavia, come a volte questo processo non si compia correttamente per la presenza di una zona pellucida particolarmente spessa e di maggior consistenza, rilevabile in presenza di ovociti da donne di età avanzata; in modo analogo è stato ipotizzato come in vivo tale condizione sia associata ad una carente produzione di sostanze enzimatiche nei tessuti circostanti ed embrionari che servono all’interazione con l’endometrio al momento dell’espansione della blastocisti.
Per superare tale ostacolo Cohen per primo nel 1988 ha reso possibile una gravidanza insorta dopo hatching assistito, ovvero distruzione artificiale della zona pellucida, eseguita prima del transfer in utero dell’embrione allo stato di blastocisti.
Sono state proposte numerose tecniche di dissezione parziale con creazione di un varco completo attraverso lo spessore della zona pellucida, rimozione totale o assottigliamento o drilling della stessa che prevedono una modalità meccanica (con ago vitreo di micromanipolazione), chimica (con soluzione acida di Thyrode), enzimatica, con l’impiego del laser o con la tecnologia piezo-elettrica.
È fondamentale che la procedura venga eseguita da biologi esperti per evitare il potenziale danno termico, secondario essenzialmente all’impiego della tecnologia laser, minimizzare il tempo di permanenza degli embrioni al di fuori dell’incubatore ed ottimizzare la metodologia per ridurre le variazioni di pH e temperatura che possono inficiare lo sviluppo dell’embrione.
Sebbene il potenziale effetto dell’hatching assistito sulla percentuale di impianto e di gravidanza sia ancora oggetto di studio è noto come tale procedura debba essere eseguita in casi selezionati rappresentati dalla presenza di una zona pellucida particolarmente spessa e soprattutto in condizioni cliniche quali:
- donne di età superiore a 37 anni che si sottopongono a cicli di FIVET omologhe;
- donne con ridotta riserva ovarica (FSH basale elevato, basso AMH e ridotto numero di follicoli antrali al conteggio ecografico);
- ripetuti fallimenti dopo tre o più transferts embrionari;
- dopo ripetuti cicli di fecondazione in cui gli embrioni presentano scarsa qualità (divisione cellulare molto lenta o con eccessiva frammentazione).
Quando l’hatching assistito viene impiegato nelle condizioni sopraindicate è possibile osservare un incremento delle percentuali di gravidanza rispetto a procedure di FIV-ET senza hatching assistito, presumibilmente conseguente ad una più elevata capacità di impianto embrionale.